3. Composición de la materia: Estructuras cristalinas
Todos los metales, excepto el mercurio, se encuentran en estado sólido a temperatura ambiente.
Esto se debe a que sus átomos ocupan unas posiciones espaciales de equilibrio predeterminadas, y a estas posiciones espaciales de equilibrio las llamamos redes cristalinas.
- Red cúbica centrada en el cuerpo (BCC)
- Red cúbica centrada en las caras (FCC)
- Red hexagonal compacta (HC)
Red cúbica centrada en el cuerpo, BCC. (Body Centered Cube)
Los átomos conforman una estructura con forma de cubo y en ella un átomo ocupa el centro geométrico del cubo y otros ocupan cada uno de los ocho vértices.

|
| Imagen 33. Wikimedia.Creative Commons |
Como hemos visto, en este tipo de redes un átomo ocupa el centro geométrico del cubo y otros ocupan cada uno de los ocho vértices.
Cada uno de estos ocho átomos pertenecen, al mismo tiempo, a cada uno de los ocho cubos que comparten el vértice. Por lo tanto, cada cristal de esta red tiene realmente el equivalente a dos átomos.
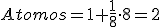
Metales que cristalizan en este sistema son, por ejemplo, hierro a, cromo, titanio, molibdeno, tungsteno, niobio, vanadio, cromo, circonio, talio, sodio y potasio.
Todos ellos tienen como característica común el ser muy resistentes a la
deformación.
Red cúbica centrada en las caras, FCC. (Face Centered Cube)
En éstas un átomo ocupa el centro de cada una de las seis caras y otro ocupa cada uno de los ocho vértices.
 |
| Imagen 34. Wikimedia. Creative Commons |
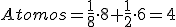
Los metales que cristalizan en esta red son fácilmente deformables.
Ejemplos de metales con estructura FCC son el hierro g, el cobre, la plata, el platino, el oro, el plomo, el níquel y el aluminio, .
Red hexagonal compacta, HC. (Hexagonal Compact),
Son aquellas en las que los átomos confoman una estructura con forma de prisma hexagonal, y presentan un átomo en el centro de cada base, un átomo en cada uno de los vértices del prisma y tres átomos más en un plano horizontal, interior al cristal.

|
| Imagen 35. Wikimedia. Creative Commons |
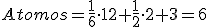
Algunos metales tienen la característica de que cambian de red de cristalización dependiendo de la temperatura a que se encuentren.
Cuando ocurre eso decimos que el metal es politrópico, y a cada uno de los sistemas en que cristaliza el metal se le llaman estados alotrópicos.
Un ejemplo de metal politrópico es el hierro.
- A partir de 1539 ºC cristaliza en la red cúbica centrada en el cuerpo (BCC) y a esta variedad alotrópica se le llama Fed
- Al llegar a los 1400 ºC cambia de red de cristalización y cristaliza en la red cúbica centrada en las caras (FCC); a esta variedad alotrópica se le llama Feg
- A partir de los 900 ºC tenemos el Feb que cristaliza de nuevo en el BCC
- A los 210 ºC aparece el Fea que, aunque no cambia de red de cristalización, adquiere propiedades magnéticas que seguirá conservando a temperatura ambiente.
En esta página tienes explicada de un forma clara y breve cómo se crea la estructura cristalina de los metales. Tienes además algunas imágenes reales de esta estructura.
http://www2.ing.puc.cl/~icm2312/apuntes/materiales/index.html

