2.1 Medida del calor transferido
El calor se mide en el S.I. en julios (J), pero también en calorías (cal). Una caloría se define como la energía necesaria para elevar un grado la temperatura de un gramo de agua. La relación entre julio y caloría es:
1 cal = 4.18 J
 |
| Imagen 7. Proyecto Newton, Creative commons |
Una experiencia clásica consiste en comunicar la misma cantidad de calor a dos recipientes que contienen igual masa de alcohol y agua.
Fíjate en la gráfica de la imagen: observa que el alcohol aumenta significativamente más rápido su temperatura, hasta que alcanza su temperatura de ebullición (78 ºC), momento en el que cesa de aumentar. Lo mismo sucede con el agua, que se calienta más lentamente y tiene un punto de ebullición más alto.
Por tanto, es necesario introducir una nueva magnitud que exprese el diferente comportamiento de las sustancias al ser calentadas.
Si se transfiere una misma cantidad de calor a dos sistemas distintos, el aumento de temperatura experimentado por cada uno de ellos no es siempre el mismo, sino que depende de su naturaleza y composición. El parámetro que relaciona el incremento de la temperatura con el calor suministrado se denomina calor específico (ce) de una sustancia, definido como la energía absorbida al calentarse un kilogramo de una sustancia y elevar su temperatura un Kelvin o un grado centígrado. Es característico de cada sustancia y se mide en el S.I. en J/(kg·K).
El aumento de temperatura viene dado por tanto por el cociente:  , de modo que el calor intercambiado puede escribirse como:
, de modo que el calor intercambiado puede escribirse como: 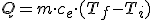
La energía transferida a un cuerpo de masa m para que su temperatura pase de una inicial (Ti) a otra final (Tf) viene dada por la expresión:
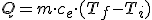
donde ce es el calor específico de la sustancia en cuestión.
Destacar también que, debido a que aparece una diferencia de temperaturas, es equivalente utilizar la escala Kelvin que la Celsius, pues según se ha visto, ambos grados son equivalentes.