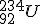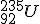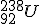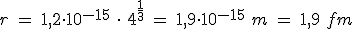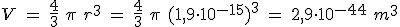1. Composición de los núcleos
El hecho de que los elementos radiactivos emitan rayos alfa y beta, ambos de naturaleza corpuscular, sugirió la idea de que los átomos estaban constituidos por partículas elementales.
 |
| Imagen 3. Cam-Ann. Creative commons. |
En 1913, los trabajos de dispersión de Rutherford llevaron a proponer que el número de cargas en el núcleo, Z, era igual al número de posición del elemento en el sistema periódico; es decir, la carga nuclear es igual al número atómico.
Como sólo se conocían los protones y los electrones y la masa de éstos era 1832 veces menor que la de aquellos, se eligió como unidad de masa atómica, u, a la masa del protón ( actualmente 1 u = 1,66·10-27 kg). Ya que la masa de un núcleo (expresada en u) está muy próxima a un número entero A, el núcleo debería estar formado por A protones. Al ser la carga del núcleo Z, Rutherford, en 1920, pensó que los núcleos poseían Z protones y A - Z pares protón-electrón (neutros) que daban en total la masa del nucleo y sugirió que constituian una partícula neutra que se denominó neutrón. Al número A se le denominó número másico.
En 1932, Chadwick demostró la existencia del neutrón, de masa muy próxima a 1 u y sin carga eléctrica, esto permitió a Heisenberg formular, en 1932, la primera teoría del núcleo.
Teoría del núcleo formulada por Heisenberg:
- El núcleo está formado por un número total de partículas elementales (neutrones y protones = nucleones) igual a su número másico, A.
- La carga nuclear Z coincide con el número de protones del núcleo. Todos los átomos de un mismo elemento tienen el mismo número de protones en el núcleo (Z).
- El número de neutrones es igual a A - Z.
- En un átomo neutro, el número de electrones (extranucleares) es igual al de protones, Z.
Los núclidos, especies nucleares particulares, se representan por:
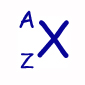
Isótopos, isóbaros e isómeros
Al comparar Z y A entre dos o más átomos se pueden establecer las siguientes denominaciones:
- Los isótopos son átomos del mismo elemento con distinto número másico. La masa de cada isótopo se denomina masa isotópica.
- Los isóbaros son átomos de distintos elementos con el mismo número másico.
- Los isómeros son átomos de igual Z y A, con distinto nivel de energía nuclear.
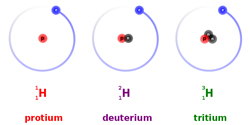 |
| Imagen 4. Erwin85. Creative commons. |
El uranio, de número atómico 92, presenta tres isótopos, el uranio-234, el uranio-235 y el uranio-238. ¿Cuál es la composición de los núcleos de estos isótopos? Escribe sus símbolos.
El tamaño del núcleo
Los radios nucleares se pueden determinar a partir de los experimentos de dispersión de partículas 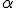 .
.
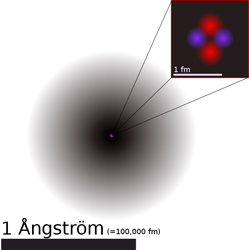 |
| Imagen 5. Yzmo. Creative commons. |
Los radios obtenidos para los diferentes núcleos están entre 10-14 y 10-15 m. El radio de un átomo es de unos 10-10 m, por lo tanto, el radio nuclear es unas 10.000 veces menor que el atómico.
Al analizar los resultados obtenidos con técnicas de dispersión de electrones, se ha propuesto una ecuación empírica que relaciona el número másico A de un átomo con el radio de su núcleo (básicamente esférico):
r = 1,2 . 10-15 A1/3 (en metros)
El tamaño del núcleo se mide en femtometros (1 fm = 10-15 m), un fm recibe el nombre de fermi, en honor al físico italiano Enrico Fermi.
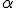 ). ¿Cuál es su volumen?
). ¿Cuál es su volumen?
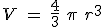
Rellena las palabras que faltan en las siguientes frases:
Número es el número de protones que contiene el núcleo, coincide con el número de sólo si el átomo es neutro.
Número es el número de nucleones del núcleo atómico; es decir, la suma total de y del núcleo.
Lo átomos del mismo elemento siempre tendrán el mismo pero puede variar su .
Átomos de un mismo elemento que tienen número de neutrones se denominan de dicho elemento.
Los de un elemento siempre tienen el número de protones .