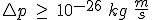4.2 Principio de Incertidumbre
En 1927, Werner Heisenberg enunció su principio de indeterminación o incertidumbre, según el cual no pueden determinarse simultáneamente la posición y el momento lineal del electrón. Una consecuencia de la dualidad onda-corpúsculo.
La posición del electrón 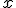 y su
momento lineal
y su
momento lineal  , sólo pueden determinarse simultáneamente con unas
indeterminaciones
, sólo pueden determinarse simultáneamente con unas
indeterminaciones 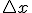 y
y 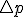 , que cumplen la relación:
, que cumplen la relación:
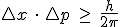
Para comprenderlo, imagina la siguiente experiencia:
 |
| Imagen 24. Radeksonic. Creative commons. |
Supón que un haz de partículas atraviesa una rendija y chocan en una pantalla. Si la anchura de la rendija es d, conoces la posición de cada partícula que pasa por la rendija con una precisión ∆x ≈d. Si las partículas no fueran ondas también, pasarían por la rendija sin modificar su momento lineal (∆p =0) , pero como son ondas, si la anchura es comparable con la longitud de onda se difractan, el haz se abre y el momento lineal modifica su componente paralela a la rendija, con lo que aparece un ∆p. Es decir, si mides con mucha precisión la posición porque la rendija es muy pequeña, mides con muy poca la velocidad (momento lineal) ya que la difracción es grande y viceversa.
El principio de incertidumbre se cumple también para otras parejas de magnitudes, llamadas magnitudes conjugadas. Son magnitudes conjugadas la energía y el tiempo y para estas el principio se expresa:
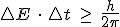
En la Mecánica clásica el
Principio de Heisenberg también se cumple aunque, como la masa de las
partículas es muy grande comparada con la constante de Planck 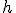 , las magnitudes
pueden determinarse con total precisión, sólo limitada por la precisión de los
aparatos de medida.
, las magnitudes
pueden determinarse con total precisión, sólo limitada por la precisión de los
aparatos de medida.
Una consecuencia del principio de indeterminación es que, si no se puede determinar a la vez la posición y la velocidad de una partícula en un instante, no se puede determinar su trayectoria y, por ejemplo, no se puede hablar de órbitas de los electrones en los átomos.
Calcula la imprecisión (incertidumbre) en la medida de la velocidad de un electrón del que conocemos su posición con una precisión de 10-15m (diámetro del electrón).
Dato: masa del electrón = 9,1∙10-31kg; constante de Planck h = 6.6∙10-34 J∙s
¿Cuál es la incertidumbre en la medida de la velocidad de un balón de futbol de 0,43 kg, si conoces su posición con una indeterminación de 1 mm?
 |
| Imagen 25. Anton. Creative commons. |
Dato: constante de Planck h = 6.6∙10-34 J∙s
 |
| Imagen 26. George W. Beran. Dominio público. |
Un virus de longitud 10-7m y 10-23kg de masa se observa con un microscopio electrónico y se determina su posición con una precisión de 10-8m. ¿Cuál es la máxima precisión con que se puede conocer su momento lineal?
Dato: constante de Planck h = 6.6∙10-34 J∙s
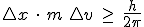 y sustituyendo:
y sustituyendo: 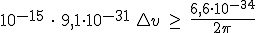 . Despejando
. Despejando 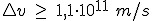
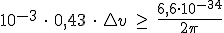 . Despejando
. Despejando 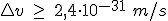
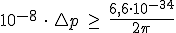 , de donde,
, de donde,