UD1. Un modelo para la materia

3º -
Ciencias de la Naturaleza
1.2 Leyes de los gases
El estudio experimental de las sustancias en estado gaseoso resulta sencillo. Por esa razón, a finales del siglo XVII ya se obtuvieron relaciones experimentales entre las magnitudes que caracterizan el estado de los gases (ley de Boyle), que se completaron posteriormente a principios del siglo XIX (leyes de Gay-Lussac).
Ley de Boyle
Cuando se comprime una jeringa hermética que contiene aire (por ejemplo, se ha sellado la punta con una gota de pegamento), se observa que el volumen que ocupa el gas disminuye conforme vamos empujando el émbolo de la jeringa, y que cada vez hemos de realizar mayor fuerza sobre la misma superficie del émbolo de la jeringa, lo que supone mayor presión.
Observa la siguiente tabla de datos de presión y volumen, medidos en una situación experimental concreta en una jeringa, así como la gráfica que las relaciona. Si te fijas, el producto de la presión por el volumen es constante; es decir, podemos afirmar que PV=constante.
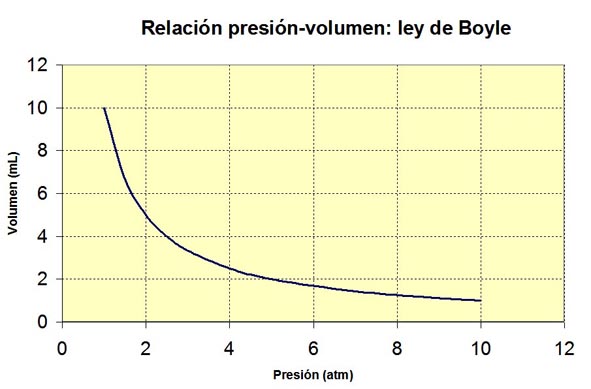
En esta experiencia no cambia la cantidad de gas que hay dentro de la jeringa ni la temperatura a la que se encuentra el gas. Al realizar la experiencia con otra cantidad de gas o a otra temperatura, se mantiene la misma relación entre presión y volumen, pero el valor de la constante varía.
Para determinar valores numéricos, solamente debemos tener en cuenta que PiVi=PfVf donde i indica la situación inicial y f la final. como de los cuatro valores sabemos tres, es fácil determinar el que queda despejando en la expresión anterior.
Ley de Boyle
Cuando se comprime una jeringa hermética que contiene aire (por ejemplo, se ha sellado la punta con una gota de pegamento), se observa que el volumen que ocupa el gas disminuye conforme vamos empujando el émbolo de la jeringa, y que cada vez hemos de realizar mayor fuerza sobre la misma superficie del émbolo de la jeringa, lo que supone mayor presión.
Observa la siguiente tabla de datos de presión y volumen, medidos en una situación experimental concreta en una jeringa, así como la gráfica que las relaciona. Si te fijas, el producto de la presión por el volumen es constante; es decir, podemos afirmar que PV=constante.
| Presión (atm) | Volumen (mL) | P*V |
| 1 | 10 | 10 |
| 2 | 5 | 10 |
| 4 | 2.5 | 10 |
| 5 | 2 | 10 |
| 10 | 1 | 10 |

Ley de Boyle
PV=constante
PiVi=PfVf

