
UD1. Estructura y propiedades de las sustancias

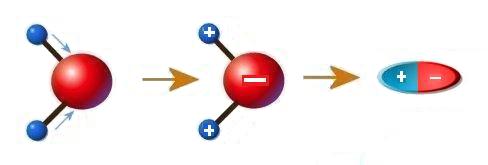
Los átomos que constituyen las moléculas de agua no se hallan colocados en línea, sino formando un ángulo.
Además, el átomo de O tira más de los electrones que comparte (tiene más tendencia a ganar electrones que los átomos de H), por lo que éstos últimos tienen cierta carga positiva y el de oxígeno carga negativa.
Esto explica la acción disolvente del agua sobre las sustancias iónicas. Las moléculas de agua tiran con su polo negativo de los iones positivos de la superficie de los cristales iónicos y con su polo positivo de los iones negativos, rompiendo los enlaces iónicos y dando lugar a la disolución de la sustancia.
Los iones, una vez separados, se quedan rodeados de moléculas de agua que impiden que se vuelvan a reagrupar.
Aquí puedes ver una animación de este proceso.
