
UD1. Estructura y propiedades de las sustancias

4º -
Física y Química
2.2 Enlace covalente


Una forma más cómoda de representar la formación de enlaces covalentes entre átomos no metálicos es utilizando lo que se conoce como diagramas de Lewis. Estos diagramas consisten en el símbolo del elemento de que se trate, rodeado por puntos, asteriscos. . . , que simbolizan los electrones de valencia.
Los diagramas de Lewis de los átomos de H, C, O y F serían:
Aunque los electrones son todos iguales, para distinguir los que pertenecen a diferentes átomos se usan símbolos diferentes.
A partir de estos diagramas, resulta sencillo averiguar los pares de electrones que deben compartir los átomos no metálicos cuando se enlazan entre ellos y también la fórmula de las sustancias formadas. Por ejemplo:
Recuerda que la configuración electrónica más estable para los átomos de hidrógeno es tener 2 electrones en la última capa (como el gas noble más próximo, el helio).
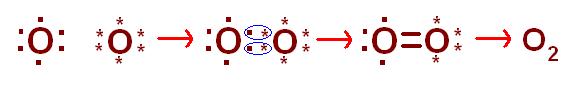
Para los átomos de oxígeno:
En este caso, los átomos de oxígeno deben compartir dos pares de electrones para conseguir el octeto en la capa de valencia, por lo que se forman dos enlaces covalentes.
