
UD2. Reacciones químicas

4º -
Física y Química
2.1 Ajuste de ecuaciones químicas
Vamos a tomar como ejemplo la reacción entre cloro (Cl2) gas y sodio (Na) sólido para obtener cloruro de sodio (NaCl) sólido, cuya ecuación química es:
Cl2(g) + Na(s) ----> NaCl(s)
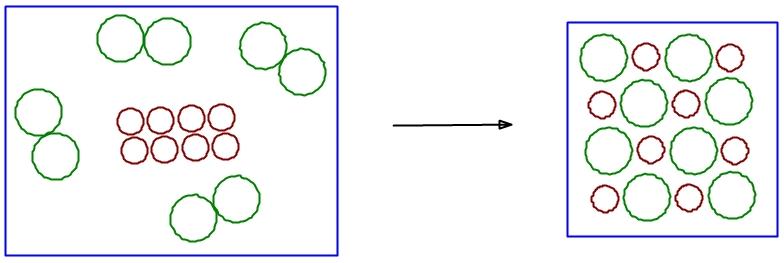
Ya sabes que en todas las reacciones químicas los átomos en los reactivos y en los productos son los mismos en tipo y en número, por lo que un esquema de partículas que represente esta reacción podría ser el siguiente:

Como ves, por cada molécula de cloro que reaccione lo harán 2 átomos de sodio.
Esto debe reflejarse en la ecuación química, y para ello hay que ajustarla poniendo delante de la fórmula de cada sustancia los coeficientes numéricos adecuados.
En este caso: Cl2 + 2 Na ----> 2 NaCl
aunque también hubiera sido correcto 2 Cl2 + 4 Na ----> 4 NaCl ó 3 Cl2 + 6 Na ----> 6 NaCl ó . . . .
Lo habitual es realizar el ajuste con los coeficientes numéricos más sencillos.
